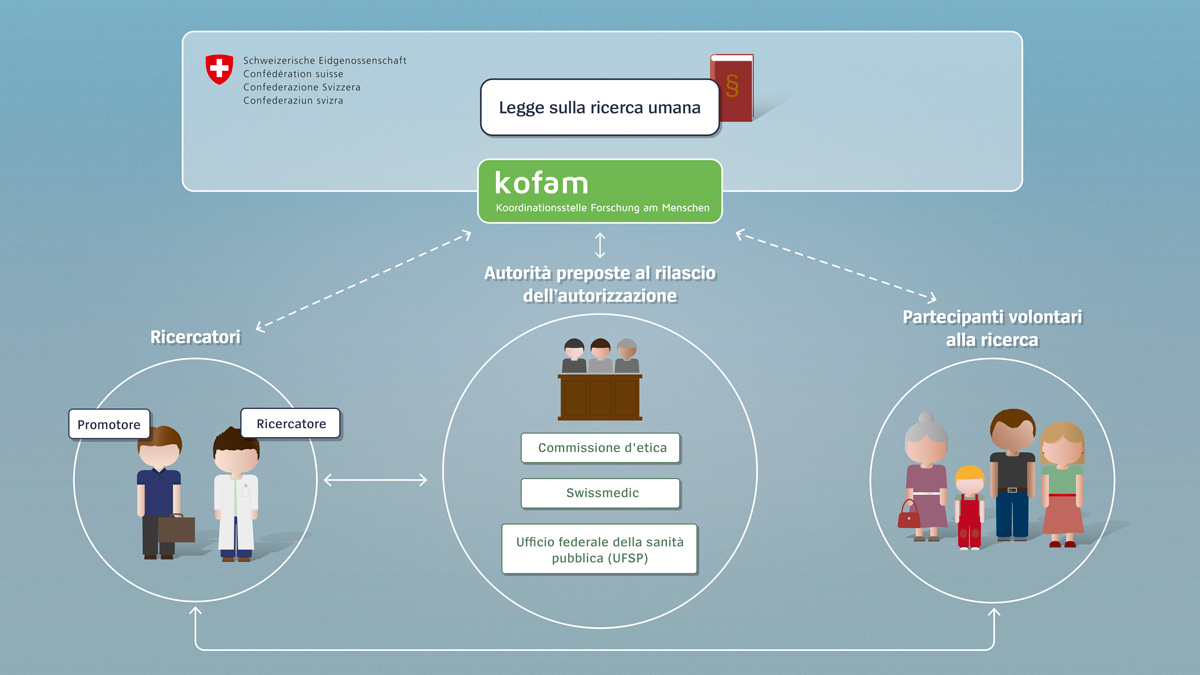
Ricercatori
Per ricercatore si intende sia lo sperimentatore - la persona che svolge effettivamente lo studio - sia il promotore, ossia l'iniziatore del progetto. Negli studi iniziati da uno sperimentatore, quest'ultimo assume anche il ruolo del promotore. Ogni progetto di ricerca che rientra nel campo d'applicazione della legge deve essere autorizzato prima del suo svolgimento. Pertanto i ricercatori sono tenuti a presentare alle autorità competenti una domanda di autorizzazione del loro progetto di ricerca.
I ricercatori hanno l’obbligo di spiegare preliminarmente il progetto di ricerca ai partecipanti e di ottenere il libero consenso di questi ultimi alla partecipazione. Durante il progetto sono inoltre obbligati a notificare gli eventi particolari alle autorità preposte all'autorizzazione.
Partecipanti alla ricerca
Per partecipanti alla ricerca si intendono le persone che partecipano a un progetto di ricerca. Essi vi prendono parte volontariamente e dopo essere stati informati dai ricercatori. Hanno il diritto di ritirarsi dal progetto in qualunque momento, ma fino a quando vi partecipano sono tenuti a rispettare le direttive.
Autorità preposte al rilascio dell'autorizzazione
Per autorità preposte al rilascio dell’autorizzazione si intendono le commissioni d’etica cantonali e l’Istituto svizzero per gli agenti terapeutici Swissmedic, in alcuni casi anche l’Ufficio federale della sanità pubblica (UFSP) e l'Ufficio federale dell’ambiente (UFAM). Le autorità esaminano le domande e rilasciano l'autorizzazione per i progetti di ricerca. Sono periodicamente informate dai ricercatori sugli eventi imprevisti e hanno la possibilità di intervenire, se necessario, e di interrompere un progetto di ricerca in casi estremi.
Confederazione
La Confederazione, nella sua veste di quarto attore, definisce le condizioni quadro con la legge sulla ricerca umana e, attraverso l’Organo di coordinamento sulla ricerca umana (kofam), assume compiti di coordinamento e mette a disposizione informazioni. In tal modo, ad esempio, i ricercatori possono informarsi sulla procedura di autorizzazione o chiunque può cercare progetti di ricerca in un apposito registro degli studi.
Maggiori informazioni
Commissioni d'etica cantonali
Le commissioni d'etica hanno il compito di esaminare gli aspetti etici, giuridici e scientifici di un progetto di ricerca. Controllano che le sperimentazioni cliniche siano svolte nel rispetto della Buona prassi clinica (Good Clinical Practice, GCP). Inoltre, sono le destinatarie di notifiche e rapporti. Se necessario, possono imporre altri obblighi o sospendere l'autorizzazione per un progetto di ricerca.
- Commissione d'etica Berna
(Cantone di Berna)
- Commissione d'etica Ginevra
(Cantone di Ginevra)
- Comitato etico della Svizzera nordoccidentale e centrale
(Cantone di Argovia, Cantone di Basilea Campagna, Cantone di Basilea Città, Cantone del Giura, Cantone di Lucerna, Cantone di Nidvaldo, Cantone di Obvaldo, Cantone di Soletta, Cantone di Svitto, Cantone di Uri, Cantone di Zugo)
- Commissione d'etica Svizzera orientale
(Cantone di San Gallo, Cantone di Appenzello Interno, Cantone di Appenzello Esterno, Cantone di Turgovia)
- Comitato etico cantonale Ticino
(Cantone del Ticino)
- Commissione d'etica Vaud
(Cantone di Vaud, Cantone di Neuchâtel, Cantone di Friburgo, Cantone di Vallese)
- Commissione d'etica Zurigo
(Cantone di Zurigo, Cantone di Glarona, Cantone dei Grigioni, Cantone di Sciaffusa, Principato del Liechtenstein)
Swissmedic
Swissmedic è l'autorità svizzera di omologazione e di vigilanza per i medicamenti e i dispositivi medici (agenti terapeutici). Per le sperimentazioni cliniche con dispositivi medici, Swissmedic verifica che venga tenuto conto dei rischi legati ai dispositivi e che i dati relativi ai dispositivi siano conformi allo stato della scienza e riportati correttamente nel protocollo. Riguardo alle sperimentazioni cliniche con medicamenti, Swissmedic ne verifica la sicurezza e la qualità. Swissmedic autorizza anche sperimentazioni cliniche della terapia genica e con espianti standardizzati. L'istituto è autorizzato a procedere a ispezioni per tutte le sperimentazioni cliniche con agenti terapeutici ed espianti standardizzati. In questo modo, l'autorità di vigilanza controlla il rispetto delle prescrizioni legali e delle direttive internazionali.
Ufficio federale della sanità pubblica
La Divisione radioprotezione dell'Ufficio federale della sanità pubblica (UFSP) è competente per l'esecuzione della legislazione sulla radioprotezione. Il suo compito consiste nel proteggere le persone e l'ambiente dai pericoli delle radiazioni ionizzanti. Se nell'ambito di un progetto di ricerca vengono effettuati esami con sorgenti radioattive non sigillate o sigillate (p. es. con radiofarmaci) la cui dose effettiva è superiore a 5 mSv l'anno, l'UFSP formula un parere in merito al rispetto della legislazione sulla radioprotezione e alla stima della dose. Per una parte delle sperimentazioni cliniche con agenti terapeutici che possono emettere radiazioni ionizzanti, l'UFSP verifica anche il rispetto della legislazione sulla radioprotezione e la stima della dose.
Prima del loro svolgimento, le sperimentazioni cliniche di trapianti di organi, tessuti e cellule di origine umana devono essere autorizzate dalla Sezione trapianti e medicina della procreazione dell'UFSP. L'UFSP può in ogni momento eseguire ispezioni di sperimentazioni cliniche di trapianti.
La Sezione sicurezza biologica dell'UFSP formula un parere sulle sperimentazioni cliniche della terapia genica, nonché su sperimentazioni cliniche con organismi geneticamente modificati o con agenti patogeni.
Ufficio federale dell'ambiente
Per le sperimentazioni cliniche della terapia genica e per quelle con organismi geneticamente modificati o con agenti patogeni, la Sezione biotecnologia dell'UFAM procede a una valutazione dei dati ambientali e formula un parere in merito alla domanda. Anche la Commissione federale per la sicurezza biologica (CFSB) esprime un parere.